消毒剂的中和剂鉴定试验
主营:
除垢剂/杀菌灭藻剂/预膜剂/缓蚀阻垢剂/粘泥剥离剂/密闭式缓蚀剂/聚丙烯酰胺/聚合氯化铝等
>更多尽在:广州市清顺环保科技有限公司 电询:13760608261 & 13668901776<
1.目 的
确定所选中和剂是否适用于拟进行的细菌和真菌杀灭试验。
2.试验器材
(1)试验菌菌悬液和菌片(见 2.1.1.2)。
(2)刻度吸管(1.0ml、5.0ml)。
(3)小平皿(4 cm~6cm 直径)。
(4)恒温水浴箱。
(5)稀释液:见附录A。
(6)胰蛋白胨大豆琼脂培养基(TSA):见附录A。
(7)电动混合器
3.试验设计原则
(1)通过所设各组试验结果综合分析,应可确定所用中和剂是否对测试消毒剂有良好的中和作用,对试验用细菌以及其恢复期培养是否有害或不良影响。
(2)在确定用何种中和剂进行鉴定试验有困难时,可对多个中和剂进行初选以确定(见本款文后【附】)。
(3)试验中所用消毒剂的浓度应以杀菌试验中使用的最高浓度为准。浓度过低,则不足以显示能否将高浓度消毒剂全部中和。
(4)鉴定试验中,消毒后去除残留消毒剂组(第2组)无菌生长,不能表明中和后受到消毒剂作用后的细菌是否能恢复生长。细菌是否复苏。此时可适当缩短作用时间重新进行试验,但作用时间最短不得少于30s,否则难以控制试验的准确性。若缩短作用时间后仍无菌生长,在排除其他原因的基础上,可适当下调杀菌试验中消毒剂浓度,再次进行中和剂鉴定试验。
(5)同一消毒剂拟对多种微生物进行杀灭试验时,应按微生物种类分别进行鉴定试验。对细菌繁殖体,在大肠杆菌(8099)、金黄色葡萄球菌(ATCC 6538)、铜绿假单胞菌(ATCC 15442)中任选其一进行试验即可;对细菌芽孢,以枯草杆菌黑色变种(ATCC 9372)芽孢进行。
当用其他特定微生物进行杀灭试验时,均应以该特定微生物进行中和剂的鉴定试验。
(6)鉴定时根据所用杀菌试验方法,使用相应的悬液或载体定量试验。
【附】中和剂初选试验
中和剂鉴定试验前,若难确定拟检测的中和剂,可通过本试验初选,而后以选中的中和剂进行正式的鉴定试验。初选操作程序如下:
(1)将0.5ml 试验菌悬液(含菌量为 1×103 cfu/ml~3×103 cfu/ml)加入含 4.5ml 中和剂试管中,混匀,作用30min后,取1.0ml接种平皿,用TSA倾注法培养。
(2)将0.5ml 试验菌悬液(含菌量为 1×103 cfu/ml~3×103 cfu/ml)加入含 4.5ml中和产物试管中,混匀,作用30min后,取1.0ml接种平皿,用TSA倾注法培养。
(3)试验同时设阳性对照组。阳性对照组以 0.5ml 菌悬液加入含 4.5ml 稀释液试管中,混匀,作用30min后,取1.0ml接种平皿,用TSA倾注法培养。
当3组平板上长出的菌落数接近,如果以阳性对照组为标准(X),前两组长菌数为(X±50%X)以内,可进行正式的鉴定试验。
4.试验分组
第1组 消毒剂 + 菌悬液 →培养
观察消毒剂对试验菌有无杀灭或抑制能力。
第2组 (消毒剂 + 菌悬液) + 中和剂 → 培养
观察残留消毒剂被中和后受到清毒剂作用后的试验菌是否能恢复生长。
第3组 中和剂 + 菌悬液 → 培养
观察中和剂是否抑菌。
第4组 (消毒剂 + 中和剂)+ 菌液 → 培养
观察中和产物,或未被完全中和的残留消毒剂对试验菌的生长繁殖是否有影响。
第5组 稀释液 + 菌悬液 → 培养
作为菌数对照。
第6组 稀释液 + 中和剂 + 培养基 → 培养
作为阴性对照。
5.中和剂悬液定量鉴定试验操作程序
根据试验分组,准备足量试管和平皿,依次进行编号。将消毒剂按所需浓度配制好后,置20℃±1℃水浴中待用。
按2.1.1.2制备试验菌悬液。取2.0ml试验菌悬液于试管中,加入2.0ml有机干扰物质,制成含有机干扰物质的菌悬液,置20℃±1℃水浴中备用。
(1)第 1 组。吸取1.0ml含有机干扰物质的试验菌悬液于试管内,置20℃±1℃ 水浴中 5min 后,再吸加4.0ml消毒剂于试管内,混匀。作用至预定时间,吸此样液 0.5ml 加于含有 4.5ml 稀释液的试管中,混匀。吸取该最终样液1.0ml,接种于平皿中,做活菌培养计数。
(2)第2组。吸取1.0ml含有机干扰物质试验菌悬液于试管内,置 20℃±1℃ 水浴中 5min 后,再吸加4.0ml消毒剂于试管内,混匀。作用至预定时间,吸此样液 0.5ml 加于含 4.5ml 中和剂溶液管中,混匀,作用10min。吸取该最终样液1.0ml,接种于平皿中,做活菌培养计数。
如平板生长菌落数均超过 300 个,应以稀释液对上述最终样液作适宜稀释后,再次进行活菌培养计数。
(3)第 3 组。吸取0.1ml含有机干扰物质的试验菌悬液于试管内,置 20℃±1℃ 水浴中 5min 后,加入0.4ml硬水,混匀。加入4.5ml中和剂,作用10min。用中和剂做10倍系列稀释,选适宜稀释度悬液,各吸取 1.0ml,分别接种于平皿中,做活菌培养计数。
(4)第 4 组。吸取0.1ml含有机干扰物质的试验菌悬液于试管内,置 20℃±1℃ 水浴中 5min 后,吸加4.9ml中和产物溶液(以0.4ml消毒剂加4.5ml中和剂,作用 10min 配制而成)于试管内,混匀。作用10min,吸取该最终样液 0.5ml,用中和产物溶液做 10 倍系列稀释,选适宜稀释度悬液,各吸取 1.0ml,分别接种于平皿中,做活菌培养计数。
(5)第5组。吸取0.1ml含有机干扰物质的试验菌悬液于试管内,置20℃±1℃ 水浴中5min 后,吸加0.4ml硬水于试管内,混匀。加入4.5ml稀释液,作用 10min ,用稀释液做10倍系列稀释,选适宜稀释度悬液,各吸取 1.0ml,分别接种于平皿中,做活菌培养计数。
(6)第 6 组。分别吸取稀释液、中和剂和硬水各1.0ml于同一无菌平皿内,倒入上述试验同批次的培养基25ml,培养观察。如出现细菌生长,可能提示试验材料或操作过程中有污染。应重新进行试验。
6.中和剂载体定量鉴定试验操作程序
根据试验分组,准备足量试管和平皿,依次进行编号。各组分别用适宜大小容量的无菌定量吸管按以下程序吸取或添加试剂和试验样本。
(1)第1组。吸取消毒剂5.0ml于无菌小平皿内,将其置20℃±1℃水浴中5min后,用无菌镊子夹入一菌片,并使浸透于消毒液中。待作用至试验预定的时间,立即用无菌镊子取出菌片移入含5.0ml稀释液试管中,作用10min。用电动混合器混合20s,或将试管振打80次,吸取该最终样液 1.0ml,接种于平皿中,做活菌培养计数。
(2)第 2 组。吸取消毒剂 5.0ml 于无菌小平皿内,将其置 20℃±1℃ 水浴中 5min 后,用无菌镊子夹入一菌片,并使浸透于消毒液中,待作用至试验预定时间,立即用无菌镊子取出菌片移入含 5.0ml 中和剂试管中,用电动混合器混合20s,或将试管振打80 次。作用10min,吸取该最终样液1.0ml,分别接种于各平皿中,做活菌培养计数。
如平板生长菌落数均超过 300个, 应重新吸取该最终样液 0.5ml,用稀释液做适当稀释,选适宜稀释度悬液,吸取1.0ml,分别接种于平皿中,做活菌培养计数。
(3)第 3 组。吸取中和剂 5.0ml 于无菌小平皿中,将其置 20℃±1℃ 水浴中 5min 后,用无菌镊子夹入 1 菌片,并使浸透于中和剂内,作用 10min。立即用无菌镊子取出菌片移入含5.0 ml 中和剂试管中,用电动混合器混合20s,或将试管振打80 次,混匀。吸取该最终样液 1.0ml,用中和剂做 10 倍系列稀释,选适宜稀释度悬液,吸取 1.0ml,分别接种于平皿中,做活菌培养计数。
(4)第 4 组。 吸取中和产物溶液 (以一片浸有消毒剂的载体置 5.0ml 中和剂内,作用10min) 5.0ml 于无菌小平皿内,将其置 20℃±1℃ 水浴中 5min 后,用无菌镊子夹入 1 菌片,并使浸透于中和产物溶液中。作用 10min,用无菌镊子取出菌片,移入含 5.0ml 中和产物溶液的试管中,用电动混合器混合20s,或将试管振打 80 次,混匀。吸取该最终样液0.5ml,用中和产物溶液做10 倍系列稀释,选适宜稀释度悬液,吸取 1.0ml,分别接种于平皿中,做活菌培养计数。
(5)第 5 组。吸取稀释液 5.0ml 于无菌小平皿内,将其置 20℃±1℃ 水浴中 5min 后, 用无菌镊子夹入 1 菌片,并使浸透于稀释液中。作用10min,立即用无菌镊子取出菌片移入含 5.0ml 稀释液的试管中,用电动混合器混合20s,或将试管振打 80 次,混匀。吸取该最终样液0.5ml,用稀释液 做10倍系列稀释,选适宜稀释度悬液,吸取 1.0ml,分别接种于平皿中,做活菌培养计数。
(6)第 6 组。分别吸取稀释液与中和剂各1.0ml于同一无菌小平皿内,倒入上述试验同批次的培养基15ml~20ml,培养观察。如出现细菌生长,提示试验材料或操作过程中可能有污染。应重新进行试验。
7.评价规定
试验结果符合以下全部条件,所测中和剂可判为合格:
(1) 第 1 组无试验菌,或仅有极少数试验菌菌落生长。
(2) 第 2 组有较第 1 组为多,但较第 3、4、5(组)为少的试验菌菌落生长,并符合表 2-1 要求者。
表 2-1 中和剂鉴定试验合格标准中对第 1 组与第 2 组菌落数的要求
|
第 1 组平板平均菌落数 |
第 2 组平板平均菌落数 |
|
0 |
>5 |
|
X(1~10) |
>(X + 5) |
|
Y(>10) |
>(Y + 0.5 Y) |
注:对抑菌作用不明显消毒剂(如乙醇)所用中和剂的鉴定试验中,当第 1 组与第 2 组菌落数相近,难以达到本表要求时,可根据具体情况另行作出判断和评价。
(3) 第 3、4、5(组)有相似量试验菌生长,悬液试验在1×107 cfu/ml~5×107 cfu/ml之间,载体试验在 5×105 cfu/片~5×106 cfu/片 之间。其组间菌落数误差率应不超过 15%。第3、4、5 组间菌落数误差率计算公式其计算公式如下。
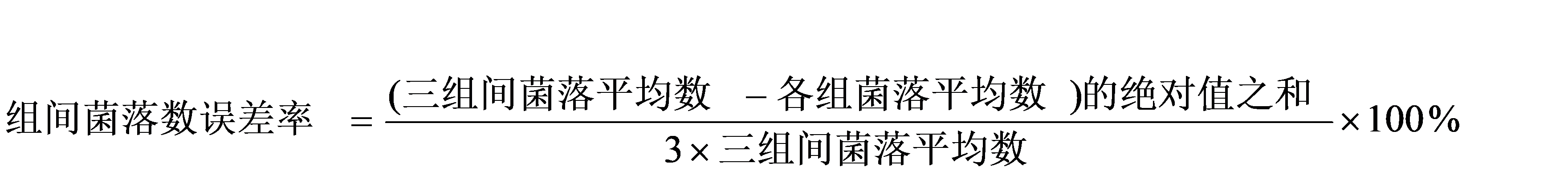
 (4)第6组无菌生长。否则,说明试剂有污染,应更换无污染的试剂重新进行试验。
(4)第6组无菌生长。否则,说明试剂有污染,应更换无污染的试剂重新进行试验。
(5)连续 3 次试验取得合格评价。
8.注意事项
(1)试验所分各组均有其特定意义,不得任意删减。
(2)严守无菌操作,保持试液和器材的无菌,注意更换吸管,以防止沾染影响试验的准确性。
(3)在计算微生物浓度时,须考虑其稀释倍数。
(4)试验组序应按本规范所列排列。

